李毓龙实验室Neuron报道新升级第二代去甲肾上腺素探针助力活体神经递质研究
去甲肾上腺素(Norepinephrine, NE)是中枢和外周神经系统中的一种至关重要的单胺类神经递质。在大脑中,NE主要由蓝斑(Locus coeruleus,LC)的神经元产生,NE能神经元广泛投射到整个大脑,影响警觉性、觉醒状态以及学习和记忆等过程。此外,NE还参与调节心率、血压等自主功能,以及应对压力的生理反应。在临床上,NE的异常释放与多种精神和神经性疾病的发展有关,如抑郁症、注意力缺陷多动障碍(ADHD)和焦虑症等。因此,在活体动物中以高灵敏度和高时空分辨率监测NE的动态变化对解析NE参与生理及病理过程的机制至关重要。尽管此前由李毓龙教授的研究团队开发的第一代可遗传编码的NE探针首次实现了对NE的检测,但其有限的灵敏度和信噪比使得在体应用存在诸多障碍。
2024年3月27日,北京大学生命科学学院、IDG麦戈文脑科学研究所、北大-清华生命科学联合中心李毓龙实验室在Neuron杂志在线发表了题为“Monitoring norepinephrine release in vivo using next-generation GRABNE sensors”的研究论文。该研究基于GRAB探针策略(GPCR-Activation Based Sensor),成功优化了二代绿色荧光NE探针,并构建了一个新型的Cre依赖型双荧光探针表达的转基因小鼠品系,实现了在活体小鼠的多个脑区和多种行为范式下,同时且可靠地检测NE和钙信号。

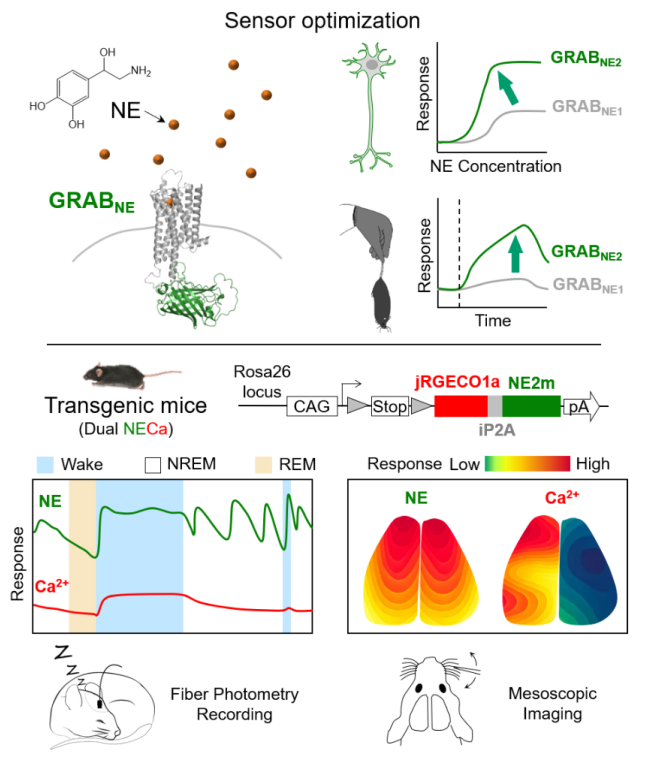
第二代去甲肾上腺素荧光探针
通过改造G蛋白偶联受体和循环重排的绿色荧光蛋白,优化的第二代NE荧光探针(包括中等亲和力版本的GRABNE2m和高等亲和力版本的GRABNE2h)在离体HEK细胞与原代神经元中表现出比第一代探针更高的灵敏度。令人振奋的是,在离体系统中对探针信号的优化成功地在活体检测系统中得到证实,优化的第二代NE荧光探针在检测由光遗传学和行为学刺激触发的蓝斑和外侧下丘脑(Lateral Hypothalamus,LH)中NE释放时,显示出高于一代NE探针5倍的荧光信号变化。此外,由于NE和另一种单胺类神经递质多巴胺(Dopamine, DA)在结构上的差异仅为一个羟基,传统的活体检测方法通常难以区分它们。幸运的是,二代NE荧光探针对NE表现出较高的分子选择性。研究表明,在小鼠体内,GRABNE2m可以检测到光遗传学刺激下神经元释放的NE,而无法检测到DA,进一步证明了该探针在精确检测神经递质动态方面的巨大潜力。
该研究不仅仅局限于探针的开发。研究团队还构建了一种新型的Cre依赖型转基因小鼠品系,能够利用Cre-LoxP系统表达两种荧光探针(绿色荧光GRABNE2m和红色荧光钙探针jRGECO1a)。结合标记不同细胞类型的Cre病毒或Cre转基因鼠,这一工具鼠可实现双色成像,同时且更为可靠地监测NE和钙信号的动态变化,将有机会为不同生理状态下的神经调控机制提供全新的见解。利用双色光纤记录和介观大视场成像技术,研究团队还揭示了在睡眠觉醒、感觉处理和运动过程中,活体小鼠中NE和钙的细胞类型特异的时空动态。这项研究揭示了在不同生理状态下,机体内具有多样化的神经调控机制。
综上所述,李毓龙教授课题组开发的第二代去甲肾上腺素荧光探针(GRABNE2m和GRABNE2h)凭借其高灵敏度和优异的选择性,为在活体条件下对NE的监测提供了更加准确的工具。通过构建的新型Cre依赖型转基因小鼠品系,实现了对NE和钙信号的双色成像与同步监测。李毓龙教授课题组的新成果为将来研究去甲肾上腺素神经调控及其对行为和神经障碍影响奠定了基础。有了这些先进的工具,研究人员能够更好地监测和解读实时变化的神经递质复杂活动,为我们理解大脑功能开辟了新的疆域。
北京大学生命科学学院冯杰思博士为本文第一作者,李毓龙教授和冯杰思博士为共同通讯作者,李毓龙课题组董辉博士(现为上海交通大学医学院松江研究院青年研究员)、邓飞博士(现为深圳湾实验室分子生理学研究所博士后)、王欢博士、李国川、蔡儒仪等对文章做出了重要贡献。该工作得到了纽约大学林大宇研究组、美国国立卫生研究院崔国红研究组及清华大学自动化系谢浩博士、庄超玮博士等的通力合作。研究得到了国家重点研发计划、国家自然科学基金、膜生物学国家重点实验室、北大-清华生命科学联合中心、生命医学峰基金、宋晨枫与高欣欣公益基金会、新基石科学基金会等机构和经费的大力支持。
原文链接
https://doi.org/10.1016/j.neuron.2024.03.001