瞿佳男:中枢神经系统中的活体高分辨率成像:大脑、视网膜和脊髓
撰稿:傅升韪,审核:李毓龙
2026年1月5日下午,应北京大学IDG麦戈文脑科学研究所李毓龙教授邀请,香港科技大学瞿佳男教授在金光生命科学楼邓祐才报告厅带来了一场题为“In Vivo High-Resolution Imaging in the CNS: Brain, Retina, and Spinal Cord”的精彩报告,系统介绍了其课题组近年来在活体高分辨率成像技术方面取得的重要进展。

【概要】
在过去的几十年中,生物光学成像技术、基因编码荧光蛋白与多光子显微镜的飞速发展,极大推动了神经科学领域对活体动物细胞及亚细胞尺度生理活动的研究。共聚焦与多光子荧光显微镜在活体光学成像中占据关键地位,结合各类荧光蛋白与化学荧光分子,不仅能够实现活体动物大脑神经元精细形态结构的高分辨率成像,还可以在多时空尺度上对动态神经活动进行实时、长期的连续记录,从而为神经环路连接和大脑功能机制的研究提供核心技术支撑。
瞿佳男教授现任香港科技大学电子及计算机工程学系教授,是美国光学学会(OSA)会士和国际光学工程学会(SPIE)会士,其团队长期致力于神经科学成像技术的开发,在活体脑成像和自适应光学显微技术等领域取得多项突破。在本次报告中,瞿教授详细介绍了其团队近期开发的多项中枢神经系统活体成像技术及相关应用。
【精彩回顾】
自适应光学双光子显微镜助力高分辨率活体视网膜功能成像
作为中枢神经系统中唯一可以通过光学手段实现无创成像的组成部分,视网膜一直是生物活体成像研究的重要对象之一。然而,即便采用双光子显微镜成像,眼球本身引入的光学像差畸变仍严重限制了视网膜单细胞分辨率成像质量。
自适应光学(adaptive optics,AO)最初用于天文望远镜中大气像差的矫正,近年来逐渐被引入生物光学成像领域。研究组通过将AO系统引入到双光子显微镜当中,利用电子倍增CCD(electron multiplying charge-coupled devices,EMCCD)作为波前传感器,将待成像区域的双光子荧光作为AO中的导星(guide star)信号,实时测量并反馈波前像差,通过可变形反射镜(deformable mirror,DM)对畸变进行校正,构建了自适应光学双光子激发显微镜(adaptive optics two-photon excitation fluorescence microscopy,AO-TPEFM)1。此外,系统中引入电可调谐透镜(electrically tunable lens,ETL)以补偿小鼠眼球的高屈光度,实现精准快速的焦面调节。借助这套系统,原先受到组织像差影响无法清晰成像的各层视网膜神经元都能得到更高分辨率的图像,包括神经纤维层(NFL)、神经节细胞层(GCL)、内网状层(IPL)的视网膜神经节细胞(retinal ganglion cell,RGCs),以及内核层(INL)的双极细胞等。同时还可以清晰成像微血管和神经元网络的精细结构(图1)。
结合绿色荧光钙探针GCaMP6s及荧光血管染料埃文斯蓝(Evans blue),研究组进一步实现了活体小鼠视网膜神经节细胞在不同刺激条件下的钙活动实时成像,并对血流速度进行了精准测量。该系统还被成功运用于青光眼动物模型的活体研究中2。通过在硅油诱导青光眼的不同时期进行亚细胞分辨率成像,系统性揭示了视网膜微血管循环、小胶质细胞和神经节细胞在疾病进展过程中的病理和功能变化。

图1 自适应光学双光子显微镜实现小鼠视网膜亚细胞分辨率成像1
自适应光学三光子显微镜实现清醒小鼠完整颅骨下皮层成像
大脑是中枢神经系统研究的核心对象,而在清醒动物中实现非侵入式、高分辨率的大脑活体成像始终是该领域面临的重大挑战。传统光学成像通常需要去除或者磨薄颅骨,存在明显的组织损伤和免疫反应风险。此外,大脑组织本身引入的散射和像差也严重限制了成像深度和分辨率。为了实现完整颅骨下的大脑成像,研究组开发了“模拟锁相相位检测焦点感测与整形”(analog lock-in phase detection focus sensing and shaping,ALPHA-FSS/α-FSS)技术,并将其与三光子显微镜相结合3。该方法通过对激发光相位进行特定调制,结合相敏探测方法对生物组织引入的各类像差进行快速精确测量与校正,从而有效提高成像信噪比。
此外,α-FSS还结合了遥距调焦共轭自适应光学技术(conjugate AO with remote focusing,CAO-RF),进一步扩大了像差校准的有效范围和高分辨成像的可用视场。利用1300 nm波长的飞秒脉冲激光作为三光子显微成像光源,该系统可透过100 μm厚的完整颅骨在软脑膜下方750 μm深处获得皮层深部的神经元胞体、树突以及周边微血管的清晰结构(图2)。结合钙探针GCaMP6s,可直接成像皮层深部的神经元钙活动。而在Cx3Cr1-GFP转基因小鼠中,这一系统也可以成像荧光标记的小胶质细胞在精密激光损伤后的响应以及在阿尔兹海默症模型小鼠中与淀粉样斑块的形态学联系3。

图2 自适应光学α-FSS系统实现深部组织多光子成像3
在α-FSS的基础上,团队进一步发展了“多路数字复用焦点感测与整形”(multiplexing digital focus sensing and shaping,MD-FSS)技术。在清醒活动的小鼠中,传统的自适应光学方法会受运动伪影的影响,无法准确校正甚至引入额外像差;MD-FSS通过光束复用和多通道数字解调,使用8束并行扫描使测量速度提升8倍,将校正速度提升至0.1秒,并能在运动干扰下稳定测量且有效校正。结合双光子显微镜,这一系统可在清醒行为小鼠中实现软脑膜下600 μm深度的亚细胞分辨率成像4。在完整颅骨的清醒活动小鼠中,MD-FSS可用于高精度记录小胶质细胞形态,微血管血流动力学、神经血管耦合以及在躯体感觉皮层和视觉皮层神经元的钙活动(图3)。
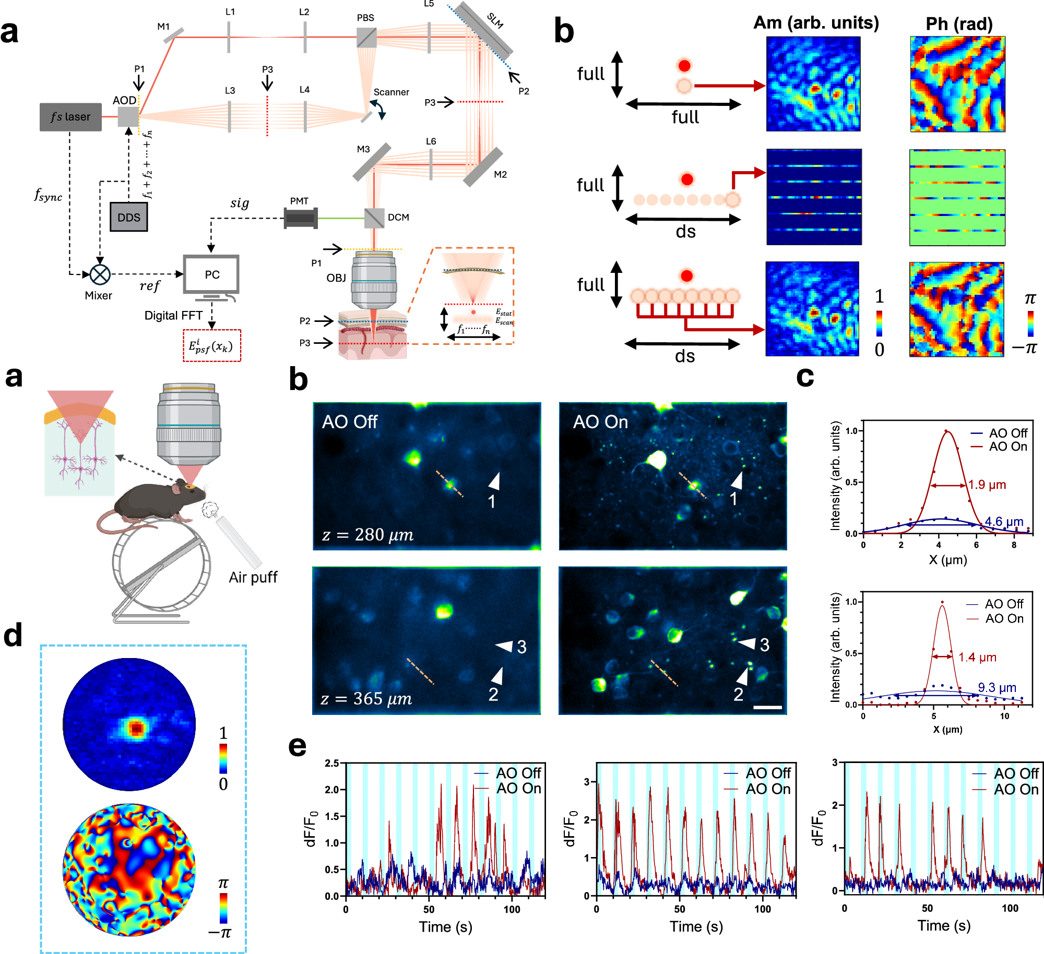
图3 应用MD-FSS系统进行清醒活动小鼠皮层神经元钙活动成像4
自适应光学双光子显微内镜实现深部脑区突触分辨率成像
针对深部脑区成像,传统梯度折射率透镜(gradient-index lens/GRIN lens)往往伴随较大的光学畸变及受限的成像视场。研究组将自适应光学引入GRIN lens成像系统,对波前像差进行补偿校正,构建了兼具高成像分辨率与大视场的自适应光学双光子显微内镜系统5。在与香港科技大学叶玉如教授课题组的合作中,该系统被成功应用于小鼠的海马脑区,实现了突触分辨率的活体成像。结合振镜扫描系统和电可调谐透镜,随机访问多平面成像方式能够对海马CA1区域神经元胞体和树突的钙活动进行高灵敏度的精细成像(图4)。
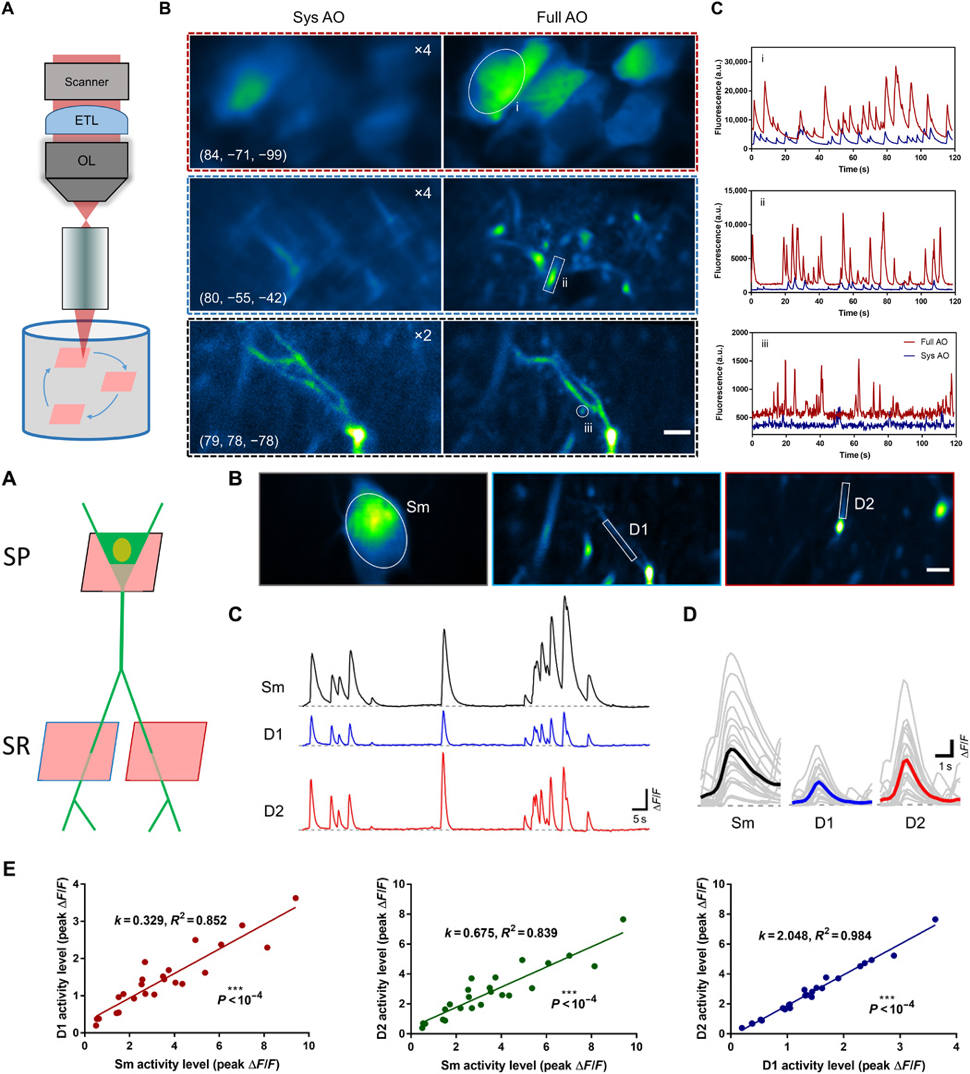
图4 自适应光学双光子显微内镜成像海马胞体及树突活动5
长期活体脊髓成像技术用于脊髓损伤机制研究
脊髓损伤往往可能引发严重且不可逆的神经功能障碍,由于缺乏适配的活体成像技术,其复杂的病理生理机制至今尚未被科学界完全阐明,极大地限制了对对治疗靶点的挖掘。为了解决这一难题,研究组与香港科技大学刘凯教授课题组合作,开发全新的活体脊髓成像技术实现对小鼠脊髓进行长期稳定的高分辨率成像。
该方法利用相邻两节脊椎骨之间的自然缝隙作为光学成像窗口,同时保留连接椎骨的黄韧带(ligamentum flavum),显著降低了手术和成像过程中引起免疫反应的风险。在此基础上为了实现更好的成像效果,研究团队引入FDA批准的X射线造影剂碘克沙醇(iodixanol)进行折射率匹配,实现成像窗口的光学透明化6。
针对脊髓中不同组成成分的成像需求,研究组结合双光子显微镜、受激拉曼散射(stimulated Raman scattering,SRS)和二次谐波产生(second harmonic generation,SHG)成像,构建了一套多模态非线性光学显微成像系统(multimodal nonlinear optical/NLO microscope)。借助该系统,研究组实现了长期稳定的脊髓活体成像,并系统揭示了轴突损伤后续过程中小胶质细胞的保护性行为及其与朗氏结(nodes of Ranvier)间的相互作用和相关分子机制(图5)7。
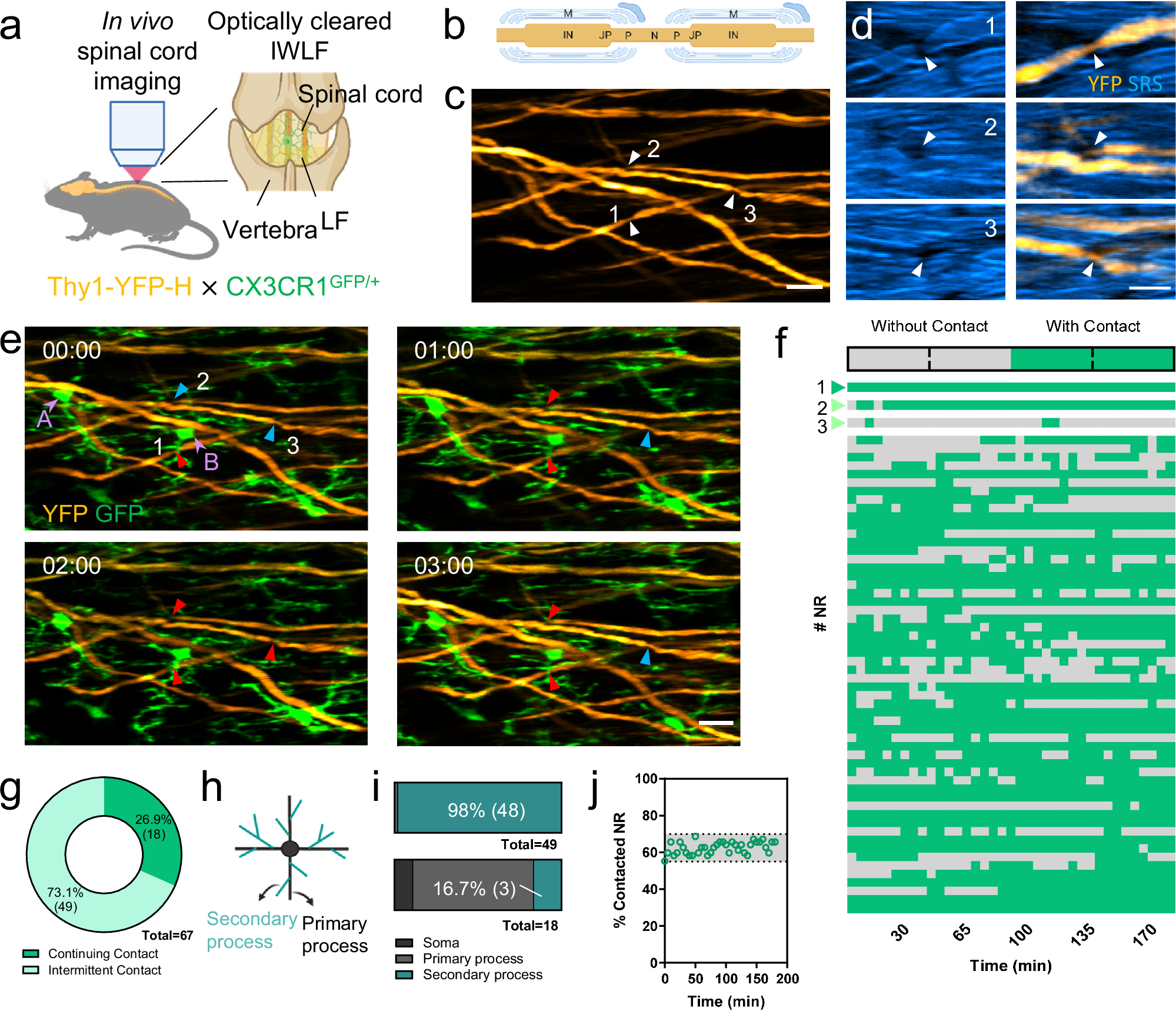
图5 通过小鼠脊髓活体成像研究小胶质细胞在轴突损伤中的作用7
上述一系列自适应光学与多模态成像技术的创新性发展,显著提升了中枢神经系统活体结构与功能成像的时空分辨率,为深入探索复杂的脑功能及疾病相关干预手段带来全新的发现和机遇。
参考文献
1. Qin, Z. et al. Adaptive optics two-photon microscopy enables near-diffraction-limited and functional retinal imaging in vivo. Light Sci Appl 9, 79 (2020).
2. Fu, Y. et al. Dynamic retinal pathology in glaucoma progression revealed by high-resolution functional imaging in vivo. Laser & Photonics Reviews, e01801. doi:10.1002/lpor.202501801.
3. Qin, Z. et al. Deep tissue multi-photon imaging using adaptive optics with direct focus sensing and shaping. Nat Biotechnol 40, 1663–1671 (2022).
4. She, Z. et al. Rapid adaptive optics enabling near noninvasive high-resolution brain imaging in awake behaving mice. Nat Commun 16, 9167 (2025).
5. Qin, Z. et al. Adaptive optics two-photon endomicroscopy enables deep-brain imaging at synaptic resolution over large volumes. Science Advances 6, eabc6521 (2020).
6. Wu, W. et al. Long-term in vivo imaging of mouse spinal cord through an optically cleared intervertebral window. Nat Commun 13, 1959 (2022).
7. Wu, W. et al. In vivo imaging in mouse spinal cord reveals that microglia prevent degeneration of injured axons. Nat Commun 15, 8837 (2024).