陈良怡团队发现胰岛可释放β细胞决定葡萄糖刺激的胰岛素两相分泌
β细胞功能异常和胰岛素分泌关系是2型糖尿病主要因素。19世纪60年代末人们就发现,当血糖急剧上升时可以刺激胰岛素的快速短暂的第一相分泌和缓慢持续的第二相分泌。2型糖尿病初期,第一相分泌降低是β细胞功能受损的标志(PMID:11484070),其机制尚不清楚。
2024年1月26日,北京大学未来技术学院、IDG麦戈文脑科学研究所、北大-清华生命科学联合中心陈良怡教授团队,在《Nature Metabolism》杂志在线发表题为“Releasable β cells with tight Ca2+-exocytosis coupling dictate biphasic glucose-stimulated insulin secretion”的论文。研究通过活体组织荧光成像技术,在胰岛内发现了一类关键的β细胞,称为可释放β细胞(Readily releasable β cells,RRβs)。它们主导了葡萄糖刺激的胰岛素两相分泌。在ob/ob小鼠糖尿病模型中,RRβs细胞功能紊乱是糖尿病进展的重要因素。

目前公认的GSIS两相分泌机制认为,β细胞内存在不同的胰岛素囊泡库,分别参与快速和慢速的胰岛素分泌(PMID:11390882)。然而,此模型并未考虑β细胞异质性影响,如不同亚群β细胞(PMID:29559510)以及其他胰岛内分泌细胞(如α和δ细胞)的不同调控(PMID:16461897)。而探究这一问题目前最大的挑战是缺乏技术手段检测活体胰岛内不同β细胞的胰岛素分泌。
陈良怡教授课题组长期从事高时空分辨率荧光成像技术开发,探究糖尿病进程中胰岛素分泌异常的机制。在本研究中,他们利用Zn2+与胰岛素共释放的特性,采用锌离子荧光染料选择性标记胰岛素融合囊泡,结合高速转盘共聚焦显微镜,发明可同时检测胰岛内不同β细胞胰岛素囊泡分泌的方法—“锌闪烁”。利用“锌闪烁”技术,作者在单个胰岛上观察到了几百上千个胰岛素囊泡分泌事件,分析这些分泌事件的时空分布,发现β细胞的胰岛素囊泡分泌具有显著的时空异质性(图1)。
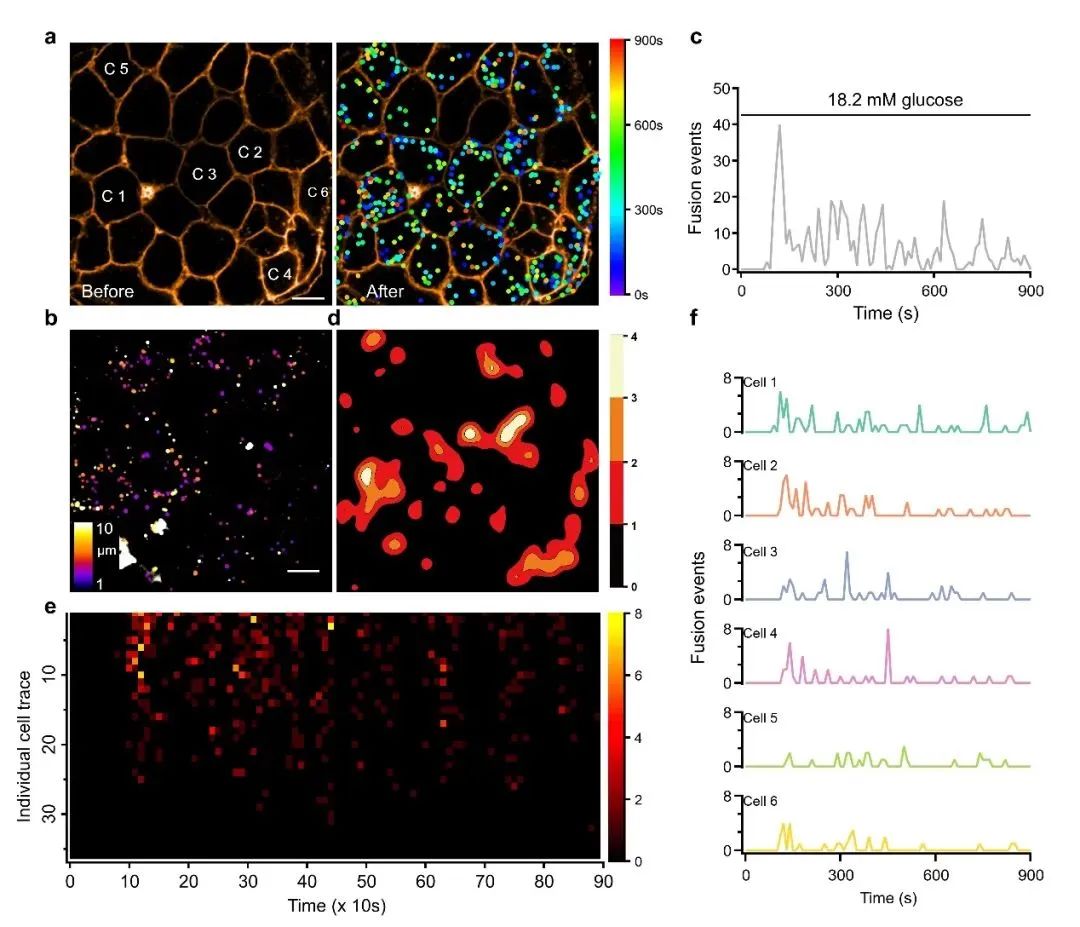
图1. 葡萄糖刺激胰岛中异质性的胰岛素分泌。a, 18.2 mM葡萄糖刺激前后胰岛素囊泡分泌事件的时空分布图。点的位置显示分泌发生的地点,颜色代表时间。b, 分泌事件在三维空间中的分布。c, 胰岛素囊泡动态分泌过程。d, 分泌事件的等高线密度图。e, 单个胰岛细胞的分泌过程。一行代表一个细胞,一个像素代表10s内分泌的囊泡个数。f, 图a中选定的六个细胞分泌动态的详图。标尺为10微米。
具体来说,生理葡萄糖刺激下只有一部分胰岛β细胞分泌胰岛素,大部分β细胞分泌很少。通过基尼系数定量评估这种异质性,发现大约40%的胰岛细胞贡献整个胰岛80%的分泌事件。因此,作者将这群分泌能力较强的β细胞定义为RRβs,其余不响应葡萄糖刺激分泌胰岛素的β细胞定义为Releasable-incompetent β cells (RIβs)。对同一个胰岛重复两轮相同葡萄糖刺激, RRβs重叠率高达83%,证明它们是胰岛中稳定存在的功能性β细胞。因此,胰岛素两相分泌由RRβs所决定,它们的同步分泌形成快速第一相,而异步分泌产生慢速第二相。
应用β细胞特异性表达Ca2+指示剂的小鼠模型Ins1-GCaMP6f小鼠和新型高性能锌离子探针PKZnR-1(PMID:34423531,北京大学陈知行教授团队合成),作者发现RRβs与RIβs在Ca2+信号上并没有明显区别。这与近期报道的基于Ca2+信号特征分类的“高功能”β细胞亚群如Hub/Leader cells (PMID: 27452146;PMID: 32694805),1st responder cells (PMID: 36099294)等明显不同,也说明Ca2+信号并不能够指代胰岛β细胞的功能。而RRβs比RIβs有更强的Ca2+-分泌偶联效率,是邻近的α细胞通过GLP-1受体和Glucagon受体促进胰岛素分泌,和δ细胞通过Somatostatin抑制胰岛素分泌共同作用的结果。
最后,在瘦素缺失的ob/ob小鼠胰岛上,其RRβs数目显著减少(4周龄50% vs 30%,8周龄42% vs 27%),而RRβ细胞的分泌功能有一个先上调再下降的过程。与正常细胞不同, ob/ob小鼠β细胞Ca2+信号从Constant 模式转变为Spike 模式, 伴随着RRβs以“Burst”的形式来分泌胰岛素。这些现象表明在胰岛水平,RRβs是胰岛素分泌调控的核心,RRβs功能失调是胰岛功能紊乱的关键环节。
综上,通过发明高分辨率胰岛成像技术,本研究发现胰岛中的RRβs,从而揭示五十年来人们一直不清楚的机制:是RRβs而不是每个胰岛β细胞中的囊泡库决定葡萄糖刺激的胰岛素两相分泌。本研究还带了另一个重要启示:单个β细胞组织成一个完整胰岛时其个体的功能受到限制;因此,两相分泌是组织成为胰岛所涌现的特性,不可能被细胞水平上、分子操纵的实验所完全阐明清楚。从这个意义来说,结合不同尺度上研究、发展在不同尺度上的高分辨率功能成像方法往往是找到生理和病理关键机制的必经之路。
该工作在线的同时,杂志以Research Briefing形式介绍了该工作(https://www.nature.com/articles/s42255-023-00964-y),此外该课题组还写了一个behind the paper的故事(下图)。

北京大学陈良怡教授和广州国家实验室刘会生研究员为本文共同通讯作者。北京大学彭晓红(原博士后,现为主管技师)、任会霞(博士后)、杨璐(助理研究员)、佟诗妍(毕业博士生)为本文共同第一作者。
原文链接
https://www.nature.com/articles/s42255-023-00962-0
https://communities.springernature.com/posts/from-a-new-method-to-a-new-mechanism-the-long-march-to-understand-how-islet-insulin-secretion-is-regulated-by-glucose-stimulation?utm_source=like_mailer&utm_medium=email&utm_campaign=notify_author_of_like