岳伟华课题组揭示非自杀性自伤行为的遗传与神经生物学机制

非自杀自伤(Non-suicidal self-injury, NSSI) 是指个体在缺乏自杀意图的前提下,反复、蓄意损伤自己身体组织的行为,在青少年群体中高发,与自杀风险、焦虑抑郁等精神问题密切相关。2025年5月9日,北京大学第六医院、IDG麦戈文脑科学研究所岳伟华课题组在Cell Press细胞出版社期刊《Cell Reports Medicine》发表题为“Multitrait GWAS of non-suicidal self-injury and the polygenetic effects on child psychopathology and brain structures”的研究论文。通过多性状全基因组关联分析联合脑发育成像数据,揭示了NSSI的遗传基础及其对儿童脑发育的深远影响。这项研究不仅为理解这一复杂行为提供了生物学解释,更为早期干预和精准治疗指明了新方向。
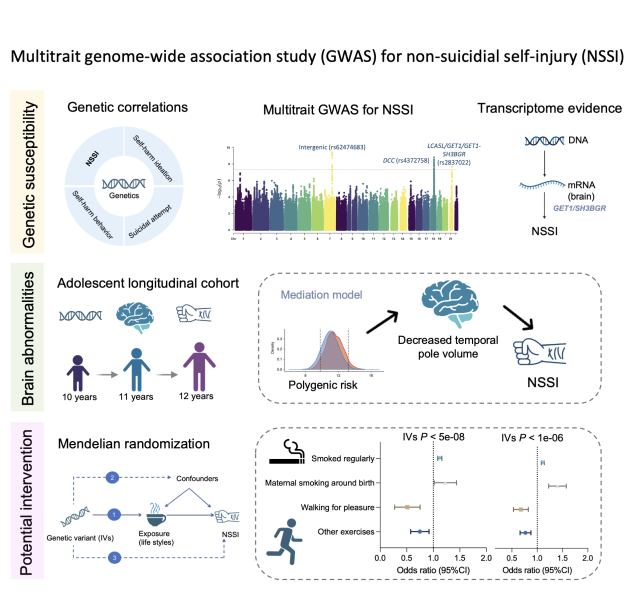
图1. 图文摘要
NSSI受遗传环境因素共同调控,尽管遗传学研究显示其遗传度达37%-59%,但此前始终未能锁定关键遗传标记。课题组利用英国生物银行分析了超10万例NSSI与健康对照的遗传数据,创新性采用多性状全基因组关联分析(MTAG),整合自伤、自杀等复杂表型数据,突破传统单表型研究局限,发现3个全基因组显著关联的NSSI遗传易感区域:DCC基因:调控神经元轴突导向,影响脑网络发育;7q31.2基因间变异:与自杀尝试存在遗传关联;GET1/SH3BGR基因座:参与蛋白质转运与细胞信号转导。通过脑转录组分析,课题组首次证实海马区GET1/SH3BGR表达水平异常升高与NSSI风险直接相关。基于贝叶斯精细定位技术,进一步锁定两个关键致病变异:SH3BGR rs4281987和GET1 rs2837022,为后续机制研究提供了精准靶点。基因通路分析揭示了NSSI的复杂致病网络,涉及Notch信号通路、蛋白质运输效率或谷氨酸能传递相关的神经发育、蛋白质稳态、突触信号及认知功能。

图2. NSSI关联遗传信号
进一步利用美国青少年脑认知发育队列近5000名青少年验证发现,具有高遗传风险的青少年在10-12岁出现NSSI行为的风险增加14%,且更易出现自杀意念、自杀尝试及内外化情绪行为问题。神经影像学证据显示,右侧颞极灰质体积减少是遗传风险影响NSSI行为的关键中介。可能提示早期遗传风险通过破坏社会情绪网络、加剧冲动-应激循环、改变疼痛情感体验等多重机制,成为NSSI行为的关键神经基质。
为了实现从实验室到公共卫生实践的转化,课题组基于孟德尔随机化分析,为临床实践提出了可操作的干预策略。研究发现,吸烟及母亲围产期吸烟使个体NSSI风险显著上升,休闲类运动(散步、游泳、健身、骑自行车、保龄球等)可降低NSSI风险。这些发现为制定分级预防策略提供了直接依据。
NSSI行为是一个需要关注的公共卫生问题。解析NSSI的潜在致病机制,为理解NSSI的生物学基础、预测高危人群及开发精准干预策略迈出关键一步。本研究结果未来还需要进一步扩大样本以及跨发育阶段进行验证,并结合单细胞测序、类脑器官模型解析风险基因的时空表达模式。最迫切的是,我们现在需要将控烟、青少年心理健康筛查纳入公共卫生体系,推动“运动处方”在社区医疗中的应用,最大程度预防NSSI发生。
北京大学第六医院博士后孙瑶瑶和博士研究生赵国瑞为该论文第一作者,北京大学第六医院岳伟华教授为末位通讯,清华大学万科公共卫生与健康学院陈润森副教授、北京大学基础医学院毕文健研究员为共同通讯作者。
Reference
Sun Y#, Zhao G#, Zhang Y, et al. Multitrait GWAS of non-suicidal self-injury and the polygenetic effects on child psychopathology and brain structures[J]. Cell Reports Medicine, 2025. May 09, 102119. DOI: 10.1016/j.xcrm.2025.102119